Камеры полагаются на системы передачи сигналов, чтобы связываться друг с другом и регулировать клеточные процессы. G-белки являются GTP-связывающими белками, которые участвуют в регуляции многих клеточных процессов. Известно два класса G-белков: мономерные G-белки (один GTPase) и гетеротримерные G-белки (три разных мономера). Белки G обычно облегчают стадию, требующую энергии. Эта энергия обеспечивается гидролизом GTP активирующим GTPase белком (GAP). Обмен ВВП на GTP катализируется гуаниновым нуклеотидным высвобождающим белком (GNRP) [Alberts et al. 1994].
G-белковые рецепторы (GPCR) являются мишенями многих фармацевтических агентов. Некоторые оценки предполагают, что от 40 до 50% продаваемых в настоящее время лекарств нацелены на GPCR, и что 40% текущих открытий лекарств сосредоточены на целях GPCR. Некоторые примеры включают в себя примеры для восстановления желудочной кислоты (ранитидин, который нацелен на гистамин H2 рецептор), мигрени (суматриптан, который нацелен на подтип серотонинового рецептора), шизофрении (оланзапин, который нацелен на рецепторы серотонина и дофамина), аллергии (дезлоратадин, который нацелен на рецепторы гистамина Одним из подходов в фармацевтических исследованиях является моделирование сигнальных путей для анализа и прогнозирования как нижестоящих эффектов, так и эффектов в связанных путях. В этом руководстве рассматриваются построение моделей и анализ цикла G-белка в пути дрожжевой феромонной реакции с помощью SimBiology® рабочий стол.
В дрожжах Saccharomyces cerevisiae передача сигналов G-белка в феромонной реакции является хорошо охарактеризованным путём передачи сигнала. Феромон, секретируемые альфа- камеры, активирует связанный с G-белком α - факторный рецептор (Ste2p) в камеры, которая приводит к различным камерам реакциям, включая остановку клеточного цикла и синтез новых белков. Авторы исследования провели количественный анализ этого цикла, сравнили регуляцию активации G-белка в дрожжевом гаплоиде дикого типа с клетками, содержащими мутации, которые придают сверхчувствительность α-фактору. Они проанализировали данные в контексте остановки клеточного цикла и феромоноиндуцированной транскрипционной активации и разработали математическую модель цикла G-белка, которую они использовали для оценки скорости активации и дезактивации активного G-белка в камере.
Системные биологи представляют биологические пути и процессы как реакции со скоростями реакции, и обрабатывают компоненты этих путей как отдельные виды.
Цикл G-белка в пути дрожжевой феромонной реакции может быть конденсирован в набор биохимических реакций. Эти реакции представляют собой комплексные реакции образования, трансформации или диссоциации, которые Yi и его коллеги [Yi et al. 2003] используется для упрощения и описания системы. В этом примере α - фактор, α - фактор рецептор и подмодули все рассматриваются как виды, участвующие в реакциях. Система может быть графически представлена следующим образом.
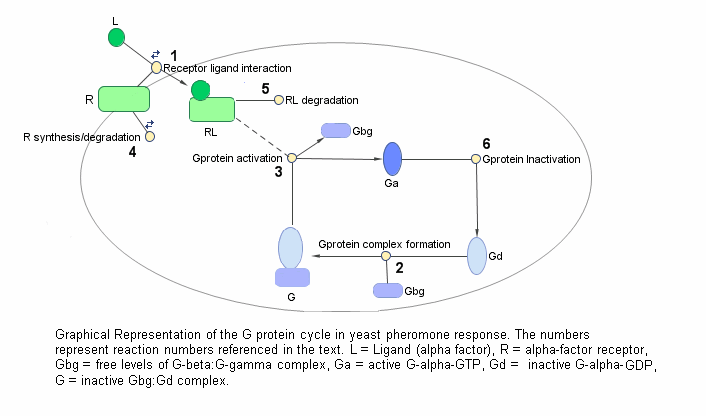
В следующей таблице показаны реакции, используемые для моделирования цикла G-белка, и соответствующие константы скорости (параметры скорости) для каждой реакции. Для обратимых реакций сначала перечисляется параметр прямой скорости.
| Нет. | Имя | Реакция | Параметры скорости |
|---|---|---|---|
| 1 | Взаимодействие рецептор-лиганд | L + R <-> RL | kRL, kRLm |
| 2 | Гетеротримерное образование G-белка | Gd + Gbg -> G | kG1 |
| 3 | Активация G-белка | RL + G -> Ga + Gbg + RL | kGa |
| 4 | Синтез и деградация рецепторов | R <-> null | kRdo, kRs |
| 5 | Деградация рецептора-лиганда | RL -> null | kRD1 |
| 6 | Инактивация G-белка | Ga -> Gd | kGd |
Обратите внимание, что в реакции 3 (активация G-белка) RL появляется с обеих сторон реакции. Это потому, что RL рассматривается как модификатор или катализатор, и модель принимает, что нет синтеза или потребления RL в этой реакции.
Авторы используют набор обыкновенных дифференциальных уравнений (ОДУ), чтобы описать систему. В программном обеспечении можно представлять биологический путь как систему биохимических реакций, и программное обеспечение создает ОДУ для вас. Кроме того, если у вас есть набор ОДУ, описывающих систему, вы можете ввести их как правила скорости. Для примера моделирования с использованием правил скорости смотрите Модель SimBiology с Правилами Скорости.
Авторы получили экспериментальные данные либо через свои собственные измерения, либо через опубликованную литературу. Как и в любой другой модели, модель цикла G-белка упрощает биологический процесс, одновременно пытаясь согласовать экспериментальные данные. Рассмотрим следующие точки:
Реакцию 2 - Связывание и образование гетеротримерного G-белкового комплекса обрабатывают как одностадийную реакцию.
Реакция 3 - Активация G-белка моделируется как одноэтапная. Факторы обмена гуаниновыми нуклеотидами (ГЭФ) не моделируются.
Реакции 3 и 6 - Параметры скорости активации и дезактивации G-белка (kGa и kGd) были оценены на основе кривых дозовой характеристики в справочной статье. Модель SimBiology, созданная в этом руководстве, непосредственно использует эти значения.
Реакции 4 и 5-Синтез и деградация рецепторов рассматриваются исключительно как две простые стадии реакции.
Реакция 6 - Дезактивация G-белка регулятором белка передачи сигналов G-белка (RGS) Sst2p моделируется как одна стадия. Sst2p не моделируется.
Реакцию моделируют с расчетной скоростью реакции 0,11 с-1) в Sst2p, содержащем штамм дикого типа. Некатализованная скорость реакции оценивается в 0,004 с-1 в штамме с делецией SST2 (sst2Δ, мутантный штамм).
Свободный ВВП, GTP и Pi в модель не включены.
В этом руководстве показано, как построить график экспериментальных данных по графику симуляции активной фракции G-белка. Можно оценить значения представляющих интерес экспериментальных данных для этого примера из координат графиков, найденных на фигура справочной бумаги [Yi et al. 2003]. Следующие значения были получены путем сравнения координат стандартов с координатами неизвестных на рисунке.
| Время | Фракция активной Ga (экспериментальная) |
|---|---|
| 0 | 0.00 |
| 10 | 0.35 |
| 30 | 0.40 |
| 60 | 0.36 |
| 110 | 0.39 |
| 210 | 0.33 |
| 300 | 0.24 |
| 450 | 0.17 |
| 600 | 0.20 |
Примечание
Функция Dimensional Analysis SimBiology не используется в этом руководстве. Для этого руководства значения всех видов преобразуются в имеющие модуль измерения molecule, и все параметры скорости преобразуются, чтобы иметь либо модуль измерения 1/second или модулей 1/(molecule*second), в зависимости от того, является ли реакция первым или вторым порядком. Вы должны оставить InitialAmountUnits поле для видов и ValueUnits окно для параметров скорости пустыми для моделей в этом руководстве.
[1] Тау-Му И, Хироаки Китано и Мелвин И. Симон. Количественная характеристика дрожжевого гетеротримерного G-белкового цикла. PNAS (2003) vol. 100, 10764-10769.
[2] Альбертс, Б., Брэй, Д., Льюис, Дж., Рафф, М., Робертс, К. и Уотсон, Дж. Д. Молекулярная биология камеры, 3-е издание, Garland Publishing, 1994.